蒸馏、重结晶——Chem带你温习基础实验操作 | 锇钔实验人 第一期
蒸馏、重结晶——Chem带你温习基础实验操作 | 锇钔实验人 第一期
金城兰州,成功摘星,下周起,全体Lzuer们就将再次回到正常的学习生活中来


写报告没重点?实验操作生疏?担心线下翻车?稍安勿躁,放宽心,因为Chem酱也已经在和实验报告的搏斗中死去了,就让Chem酱带你回温经典,克服恐惧,掌握操作,“做回自己”

一起回温实验流程,一起了解操作重点,一起吐槽实验课的三两事,实验中的酸甜苦辣尽在“锇钔实验人”
01大浪淘沙现真金——重结晶
【原理简介】
重结晶作为化学实验中的基本操作之一,是将物质溶于溶剂或熔融后,又重新从溶液或熔融体中结晶的过程,重结晶可以使不纯净的物质获得纯化,或使混合在一起的物质彼此分离。

重结晶分离纯化混合物的原理,一般是利用了混合物体系中各物种溶解度的差异。
一般来说,随着温度升高,固体混合物的溶解度都会增大,但增幅各有不同。对于混合物中的不溶杂质,可以搭配热过滤装置将杂质除去,而对于在所选溶剂均有溶解的大量目标物和少量可溶杂质,则可以通过分析温度-溶解度曲线,在较高的温度下得到目标物的纯净晶体和目标物的饱和液兼杂质的不饱和液。
若产物有旋光性,通过向热的饱和或过饱和的外消旋溶液中加入一种纯光活性异构体的晶种,创造出不对称的环境,稍微过量的与晶种相同的异构体就会优先结晶,滤去晶体后,在剩下的母液中再加入水和消旋体制成的热饱和溶液,再冷却到一定的温度,这时另一个稍微过剩的异构体就会结晶出来,从而也可以用重结晶完成对外消旋体的拆分。
【操作指北】
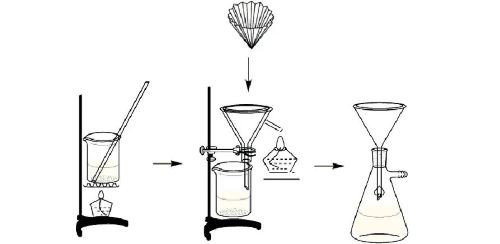
Step1.将混合物溶解于适当热溶剂中,制成近饱和的溶液

Step2.趁热过滤除去不溶性杂质

Step3.冷却滤液,产物析出

Step4.减压过滤,干燥产物

【要点分析】
1、重结晶实验,最重要的在于溶剂以及溶剂量的选择,以杂质溶解度大,产品溶解度随温度变化较大的溶剂为宜,同时溶剂不宜多加,一般能使产物完全溶解后再补加一部分即可;
2、趁热过滤步骤中,花滤纸应在不揉皱滤纸的基础上多折几层,以保障过滤效率;若无外部加热装置,要使用无颈漏斗,防止产物在漏斗颈部析出;一定要保证溶液过滤时仍为热溶液,溶液过多时,不参与过滤的液体应继续加热,否则,产物将在过滤时冷却析出,影响冷却效率并导致产品损失。
3、一般的混合物中,产品往往多于其余杂质,析出产品时要尽可能使其冷却完毕,以减少所需产物的溶解损失。
02几秋飘荡终归真——常压蒸馏
【原理简介】
常压蒸馏是在常压条件下,利用液体混合物中各组分沸点的差别,使液体混合物部分汽化并随之使蒸气部分冷凝,从而实现其所含组分的分离。也因为常压蒸馏的作用原理,常压蒸馏有一定的局限性,对待分离的液体混合物沸点差的有较高的要求,一般在30℃以上。
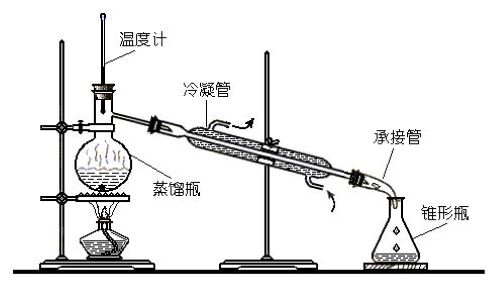
【操作指北】
Step1.按装置图搭好实验装置,在蒸馏烧瓶里加好待分离液体和沸石

Step2.接通蒸馏水,使直形冷凝管开始冷凝(若所需产物沸点高于140℃,应使用空气冷凝)

Step3.当温度计示数稳定在所需收集的产物的沸点左右时,换上干净干燥的收集瓶收集馏分(低于稳定沸点的馏头、高于产物沸点的馏尾按需要进行收集和测定)

Step4.测量馏分的体积,并妥善保存或回收

【要点分析】
1、在进行蒸馏的过程中,应注意添加沸石并通上冷凝水(或使用空气冷凝),若开始未添加沸石,应及时停止反应,待体系冷却后补加。
2、指示温度的温度计的温度泡上端应该与支管口的下沿对齐,以获得较为准确的气体温度;在产物沸点附近,一定要等待温度计示数稳定后再搜集对应物质。
3、体系不可完全封闭,否则因内部气压变大有爆炸风险。
以上就是Chem本次和大家分享的全部内容啦,祝回到实验室的同学们实验成功,操作顺利,祝没有完成预习报告的同学摆脱“苦海”,早日“上岸”

最后,也欢迎各位化学人和Chem酱分享属于自己的实验故事,面对即将到来的线下授课,让锇钔一起,冲冲冲!






